亞葉酸
此條目可參照英語維基百科相應條目來擴充。 (2024年11月16日) |
 | |
 | |
| 臨床資料 | |
|---|---|
| 讀音 | Leucovorin /ˌljuːkoʊˈvɔːrɪn/ |
| 商品名 | 許多 |
| 其他名稱 | citrovorum factor, 5-formyltetrahydrofolate |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a608038 |
| 核准狀況 | |
| 懷孕分級 |
|
| 給藥途徑 | 靜脈注射, 肌肉注射, 口服給藥 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 | |
| 藥物動力學數據 | |
| 生物利用度 | 依攝入劑量而定 |
| 血漿蛋白結合率 | ~15% |
| 生物半衰期 | 6.2小時 |
| 排泄途徑 | 腎臟 |
| 識別資訊 | |
| |
| CAS號 | 1492-18-8 |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.000.328 |
| 化學資訊 | |
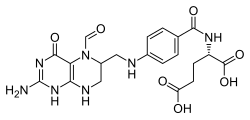
| 化學式 | C20H23N7O7 |
| 摩爾質量 | 473.45 g·mol−1 |
| 3D模型(JSmol) | |
| 熔點 | 245 °C(473 °F) decomp |
| 水溶性 | ~0.3[1] mg/mL (20 °C) |
| |
| |
亞葉酸(INN:folinic acid)俗稱活性葉酸,又名甲醯四氫葉酸 (Leucovorin),是用來減輕氨甲蝶呤和乙胺嘧啶毒性反應的藥物[2][3]。在治療大腸癌時,會同時併用5-氟尿嘧啶。也可用於治療甲醇中毒和葉酸缺乏症造成的貧血[3] [4]。此藥物有口服給藥、肌肉注射或靜脈注射等不同劑型[3]。
使用後的副作用有睡眠困難、過敏或發燒[2] [3]。一般認為,個體於懷孕期間使用對於胎兒無礙,在哺乳期間使用,對於嬰兒無安全顧慮[2]。治療貧血時,應先排除惡性貧血(如果導致貧血的真正原因是惡性貧血,而僅使用亞葉酸治療,會延誤對根本原因(可能是維生素B12缺乏所致)的診斷和治療。)[3]。亞葉酸是葉酸的一種形式,不需透過二氫葉酸還原酶活化,就能在體內產生作用[3]。
亞葉酸於1945年首次合成[5],且已名列世界衛生組織基本藥物標準清單之中[6]。
醫療用途
[編輯]
亞葉酸有口服錠劑,也有經由靜脈注射或肌肉注射的製劑。[7]
減輕氨甲蝶呤的副作用
[編輯]亞葉酸通常在氨甲蝶呤治療後給予,作為整體化療方案的一部分,它可防止骨髓抑制或減輕胃腸道黏膜發炎。但對於已存在的氨甲蝶呤引起的腎毒性,則無明顯療效。[8]
雖然亞葉酸並非氨甲蝶呤的特效解毒劑,但也可用於治療急性氨甲蝶呤過量。雖然亞葉酸的用量會根據情況調整,但必須持續給藥,直到血液中氨甲蝶呤的濃度降到每升降到5 x 10⁻⁸摩爾以下。[9]
此外,葉酸鈣有時也用於減輕氨甲蝶呤在類風濕性關節炎患者身上產生的副作用 - 如噁心、腹痛、肝檢測指數異常和口腔潰瘍。[10]
其他用途或適應症
[編輯]亞葉酸也與化療藥物5-氟尿嘧啶合用於治療大腸癌。亞葉酸在此的功能是通過抑制胸苷激酶來增強5-氟尿嘧啶的作用。 亞葉酸有時也用於預防因高劑量抗微生物二氫葉酸還原酶抑制劑(如甲氧苄啶和乙胺嘧啶)而發生的毒性作用,然而其在這些應用中的價值仍有待進一步研究。[11]它可與葉酸拮抗劑如乙胺嘧啶和磺胺嘧啶合用,來治療弓蟲性視網膜炎。
亞葉酸也用於治療腦葉酸缺乏症,單獨使用葉酸無法將腦脊髓液中的左旋甲基葉酸 (5-MTHF) 水平恢復正常。[12]
對於吡哆醇依賴性癲癇,如果使用吡哆醇或磷酸吡哆醛未能完全控制癲癇發作時,可使用亞葉酸作為輔助藥物。[13]
嚴禁將亞葉酸透過鞘內注射給藥,會有導致嚴重不良反應,甚至是死亡的風險。[14]此情況的首例發生在一位正在接受鞘內注射氨甲蝶呤以治療急性淋巴性白血病的11歲男孩身上,而導致嚴重神經毒性發生。[14]
藥物交互作用
[編輯]5-氟尿嘧啶: 如果亞葉酸和5-氟尿嘧啶同時給藥,亞葉酸鈣可能會增加與5-氟尿嘧啶相關的毒性。特別是在年長的患者中,曾出現一些不良反應,包括嚴重的腸炎、腹瀉和脫水。
複方新諾明:合併使用磺胺甲噁唑-甲氧苄啶(即複方新諾明)和亞葉酸可能存在藥物交互作用。研究顯示,亞葉酸可能會降低磺胺甲噁唑-甲氧苄啶治療卡氏肺孢子蟲導致的肺炎,這種肺炎是愛滋病患者中常見的感染。[16]
作用機轉
[編輯]亞葉酸是四氫葉酸的5-甲酰衍生物。它很容易轉化為其他還原型葉酸衍生物(例如,5,10-亞甲基四氫葉酸、左旋甲基葉酸),因此具有與葉酸相當的維生素活性。由於其轉化不需要二氫葉酸還原酶的作用,因此其作為維生素的功能不受氨甲蝶呤等藥物對該酶抑制作用的影響。這是以往對亞葉酸療法的經典觀點。然而人們在1980年代發現即使在氨甲蝶呤存在的情況下,亞葉酸鈣也能重新激活二氫葉酸還原酶本身。
科學界還不太清楚亞葉酸如何只在正常細胞中恢復某種酶(二氫葉酸還原酶)的活性,但研究認為,癌細胞中氨甲蝶呤和二氫葉酸發生的一種變化(多聚穀氨酸化)可能與這個選擇性作用有關。[17]
因此,亞葉酸在二氫葉酸還原酶受到抑制的情況下,仍能促進部分嘌呤/嘧啶的合成,使得一些正常的DNA複製過程得以進行。
亞葉酸具有右旋和左旋同分異構體。左旋亞葉酸(左旋異構體)和外消旋亞葉酸(左右兩種異構體的混合物)具有相似的療效和人體耐受性。[18]左旋亞葉酸於2008年獲得美國食品藥物管理局(FDA)批准用作醫療用途。[19]
兩位科學家H. E. Sauberlich和C. A. Baumann於1948年發現一種名為Leuconostoc citrovorum的明串球菌屬需要某種生長因子才能生長。[20]這個因子因此最初被稱為"檸檬酸發酵球菌因子"(citrovorum factor),意指它是促進L. citrovorum菌種生長的物質。當時這種物質的化學結構尚未被了解,但已確認它是葉酸的一種衍生物,並且必須先在肝臟中經過代謝轉化,才能被L. citrovorum利用。後來科學家們在培養的肝細胞中利用葉酸,並在適當濃度的抗壞血酸(維生素C)的幫助下成功合成這種檸檬酸發酵球菌因子。而且,如果在這個合成系統中同時加入甲酸鈉,會觀察到在無細胞上清液中的檸檬酸發酵球菌因子的活性會顯著增強。現在已確定這是因為甲酸鈉促進5-甲酰衍生物的生成。科學家們正是通過這種大量製備此種因子的方法,最終確定其結構,即左旋亞葉酸(5-甲酰四氫葉酸)。[21]
雖然亞葉酸是葉酸(維生素B9)的一種形式,兩者並不相同。不過亞葉酸在體內能發揮與葉酸相同的維生素功能。目前已知只有左旋葉酸及其鹽類(2S-結構)才具有生物活性。
藥物通常以其鈣鹽(葉酸鈣)或鈉鹽(葉酸鈉)的形式製備,另有甲酰四氫葉酸鈣、甲酰四氫葉酸鈉的稱法。
參考文獻
[編輯]- ^ Safety Data Sheet Folinic Acid (calcium salt) (PDF). [2018-01-25].
- ^ 2.0 2.1 2.2 British national formulary : BNF 69 69. British Medical Association. 2015: 576–577. ISBN 9780857111562.
- ^ 3.0 3.1 3.2 3.3 3.4 3.5 Leucovorin Calcium. The American Society of Health-System Pharmacists. [2016-12-08]. (原始內容存檔於2017-05-10).
- ^ Munjal YP, Sharm SK. API Textbook of Medicine, Ninth Edition, Two Volume Set. JP Medical Ltd. 2012: 1945. ISBN 9789350250747. (原始內容存檔於2017-05-10) (英語).
- ^ Sneader, Walter. Drug Discovery: A History. John Wiley & Sons. 2005: 235. ISBN 9780471899792. (原始內容存檔於2017-05-10) (英語).
- ^ World Health Organization. World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ McGuire BW, Sia LL, Leese PT, Gutierrez ML, Stokstad EL. Pharmacokinetics of leucovorin calcium after intravenous, intramuscular, and oral administration. Clinical Pharmacy. January 1988, 7 (1): 52–58. PMID 3257913.
- ^ Therapeutic Information Resources Australia (2004). Calcium Folinate (Systemic) in AUSDI: Australian Drug Information for the Health Care Professional. Castle Hill: Therapeutic Information Resources Australia.[頁碼請求]
- ^ Leucovorin (PDF). CCO Formulary. [2014-01-07]. (原始內容 (PDF)存檔於2008-10-10).
- ^ Shea B, Swinden MV, Tanjong Ghogomu E, Ortiz Z, Katchamart W, Rader T, et al. Folic acid and folinic acid for reducing side effects in patients receiving methotrexate for rheumatoid arthritis. The Cochrane Database of Systematic Reviews. May 2013, 5 (5): CD000951. PMC 7046011
 . PMID 23728635. doi:10.1002/14651858.CD000951.pub2.
. PMID 23728635. doi:10.1002/14651858.CD000951.pub2.
- ^ Trubiano JA, Grayson ML. Trimethoprim and Trimethoprim–Sulfamethoxazole (Cotrimoxazole). Grayson ML, Cosgrove S, Crowe S, Hope W, McCarthy J, Mills J, Mouton JW, Paterson D (編). Kucers' the Use of Antibiotics 7th. CRC Press. 2017: 1652. ISBN 9781498747967. doi:10.1201/9781498747967.
- ^ Gordon N. Cerebral folate deficiency. Developmental Medicine and Child Neurology. March 2009, 51 (3): 180–182. PMID 19260931. S2CID 7373721. doi:10.1111/j.1469-8749.2008.03185.x.
- ^ Kaminiów K, Pająk M, Pająk R, Paprocka J. Pyridoxine-Dependent Epilepsy and Antiquitin Deficiency Resulting in Neonatal-Onset Refractory Seizures. Brain Sciences. December 2021, 12 (1): 65. PMC 8773593
 . PMID 35053812. doi:10.3390/brainsci12010065
. PMID 35053812. doi:10.3390/brainsci12010065  .
.
- ^ 14.0 14.1 Jardine LF, Ingram LC, Bleyer WA. Intrathecal leucovorin after intrathecal methotrexate overdose. Journal of Pediatric Hematology/Oncology. August 1996, 18 (3): 302–304. PMID 8689347. S2CID 43280375. doi:10.1097/00043426-199608000-00014.
- ^ Florit-Sureda M, Conde-Estévez D, Vidal J, Montagut C. Hypersensitivity reaction caused by folinic acid administration: a case report and literature review. Journal of Chemotherapy. December 2016, 28 (6): 500–505. PMID 26042586. S2CID 25420102. doi:10.1179/1973947815Y.0000000048. hdl:10230/27696
 .
.
- ^ Razavi B, Lund B, Allen BL, Schlesinger L. Failure of trimethoprim/sulfamethoxazole prophylaxis for Pneumocystis carinii pneumonia with concurrent leucovorin use. Infection. January 2002, 30 (1): 41–42. PMID 11876516. S2CID 35513636. doi:10.1007/s15010-001-1172-0.
- ^ Goldman ID, Matherly LH. Biochemical factors in the selectivity of leucovorin rescue: selective inhibition of leucovorin reactivation of dihydrofolate reductase and leucovorin utilization in purine and pyrimidine biosynthesis by methotrexate and dihydrofolate polyglutamates. NCI Monographs. 1987, (5): 17–26. PMID 2448654.
- ^ Kovoor PA, Karim SM, Marshall JL. Is levoleucovorin an alternative to racemic leucovorin? A literature review. Clinical Colorectal Cancer. October 2009, 8 (4): 200–206. PMID 19822510. doi:10.3816/CCC.2009.n.034.
- ^ FDA Approves Levoleucovorin. Drugs.com. 2008-05-07 [2009-06-07]. (原始內容存檔於2009-07-02).
- ^ A New Form of Folic Acid-The Levconostoc Citrovorum Factor. Nutrition Reviews. 2009-04-27, 8 (9): 282–284. PMID 14775946. doi:10.1111/j.1753-4887.1950.tb02478.x (英語).
- ^ Rabinowitz, J. C., & Pricer Jr, W. E. (1956). Formimino-tetrahydrofolic acid and methenyltetrahydrofolic acid as intermediates in the formation of N10-formyltetrahydrofolic acid. Journal of the American Chemical Society, 78(21), 5702-5704.
外部連結
[編輯]- Leucovorin. MedlinePlus.
